4.1. Desplazamiento simple (sustitución simple)
Ocurre cuando un elemento reemplaza a otro en un compuesto, siguiendo la ecuación general:
Características:
Elemento más reactivo desplaza a uno menos reactivo: Se guía por la serie de reactividad de metales (ejemplo: Zn > Cu > Ag).
Tipos de sintesis simple:
Metales que desplazan hidrógeno en ácidos:
El zinc (más reactivo) libera hidrógeno gaseoso.Metales que desplazan otros metales en sales:
El hierro forma sulfato de hierro(II) y precipita cobre metálico.
Importante:
Posición en la serie de reactividad: Solo ocurre si el elemento libre es más activo que el del compuesto.
Estado de oxidación: Elementos con mayor tendencia a oxidarse (perder electrones) actúan como agentes reductores.
4.2. Desplazamiento doble (sustitución doble)
Implica el intercambio de iones entre dos compuestos, formando nuevos productos. Su ecuación general es:
Tipos de sintesis dobles:
Reacciones de neutralización: Ácido + base → sal + agua.
Reacciones de precipitación: Formación de un sólido insoluble.
El cloruro de plata (AgCl) precipita como sólido blanco.
Reglas de solubilidad:
Sales solubles: Nitratos (NO₃⁻), alcalinas (Na⁺, K⁺), amonio (NH₄⁺).
Sales insolubles: Sulfuros (S²⁻), carbonatos (CO₃²⁻), hidróxidos (OH⁻) de metales pesados.
Ejemplo:
La reacción entre sulfato de cobre (CuSO₄) y hidróxido de sodio (NaOH):
El hidróxido de cobre(II) forma un precipitado azul.
Ball, D. W., & Key, J. A. (2014, 16 septiembre). Types of Chemical Reactions: Single- and Double-Displacement Reactions. Pressbooks. https://opentextbc.ca/introductorychemistry/chapter/types-of-chemical-reactions-single-and-double-displacement-reactions/
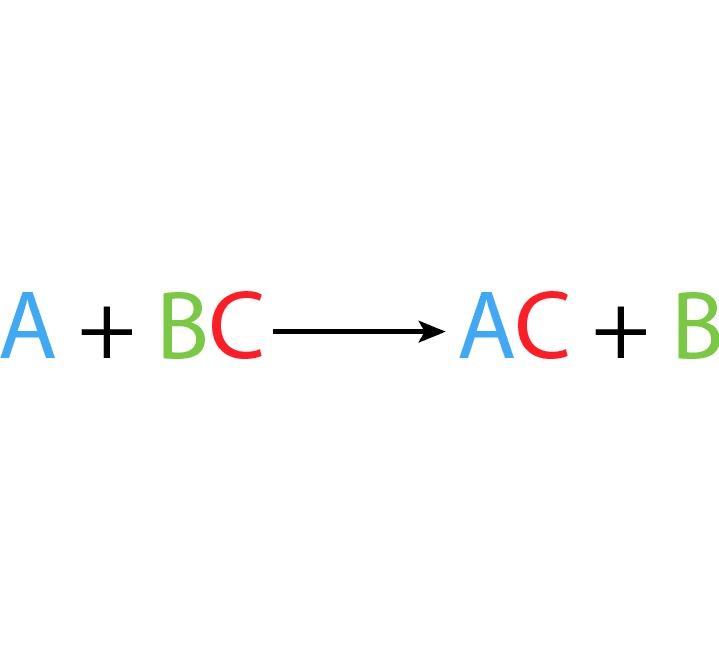

No hay comentarios:
Publicar un comentario